- Si bien la atención mundial se centra actualmente en la COVID-19 y otras enfermedades zoonóticas que saltan de los animales a los humanos, también hay padecimientos que rompen la barrera de las especies y pasan de las personas a los animales domésticos y a las especies salvajes.
- La alteración humana del planeta —la tala de bosques, el comercio legal e ilegal de fauna silvestre, el cambio climático y otras— están impulsando la escalada de interacciones antinaturales entre las especies, lo que permite que las enfermedades muten e infecten a nuevos huéspedes.
- Las enfermedades infecciosas suponen una grave amenaza para tigres, chimpancés, lobos etíopes, perros salvajes africanos y una multitud de especies amenazadas. Las enfermedades virales transmitidas por los humanos, el ganado y otros animales domésticos podrían ser el golpe de gracia para las especies en peligro que ya se tambalean al borde de la extinción.
Una asombrosa tigresa demacrada, llamada Galia, alertó a los investigadores en el extremo oriente ruso de que algo andaba muy mal. Ella, y poco después otros tigres de Amur salvajes (Panthera tigris altaica), deambulaban por las aldeas y se miraban en las carreteras, aturdidos, hambrientos y sin miedo a los humanos, un comportamiento extremadamente anormal para este felino cauteloso y reservado.
Cuando el experto en tigres Dale Miquelle lo investigó, vinculó estos misteriosos problemas neurológicos a síntomas del moquillo canino, un virus global y altamente contagioso que los tigres probablemente adquirieron al atacar a perros salvajes o huéspedes virales: martas o lobos. Galia y los otros tigres murieron.

La pandemia de COVID-19 nos ha recordado que muchos patógenos son zoonóticos y saltan de una especie a otra. Hoy en día, la atención mundial se centra en aquellos que se originan en la fauna silvestre y mutan para infectar a los humanos, el ganado y nuestras queridas mascotas. Sin embargo, muchos patógenos también saltan en la otra dirección. Humanos y animales domésticos propagan enfermedades a la fauna silvestre, dice Steve Osofsky, director del Centro de Salud de la Fauna Silvestre de Cornell in Ithaca, Nueva York.
Poca gente se da cuenta de que el simple hecho de traer humanos, vacas, cerdos, gallinas o perros a una zona salvaje, o a sus cercanías, puede acelerar la desaparición de especies en peligro.
El moquillo canino es solo un ejemplo: ha incrementado en forma sustancial las probabilidades de que al menos 500 tigres de Amur puedan desaparecer para siempre en los próximos 50 años.
“Hay una causa subyacente sorprendentemente simple”, dice Osofsky y añade: “Nuestra relación fracturada con la naturaleza salvaje a menudo se basa en una presunción de que, de alguna manera, estamos separados del resto de vida en la Tierra”.
La actividad humana está alterando rápidamente casi todos los sistemas naturales en la Tierra, tan dramáticamente que ha lanzado una nueva era geológica, el Antropoceno. Muchos de los cambios humanos —que van desde la deforestación desenfrenada, la ganadería, la agricultura y el comercio mundial hasta los viajes internacionales, el comercio de la fauna silvestre y el cambio climático— ayudan a propagar las enfermedades.
Eso se debe a que estas actividades ponen a las personas, el ganado y la fauna silvestre en estrecho contacto, lo que los expone a todos, a bacterias y virus para los que carecen de inmunidad.
En un mundo cada vez más caliente, los mosquitos, las garrapatas y otros parásitos portadores de enfermedades están expandiendo sus áreas de distribución y traen con ellos enfermedades debilitantes y mortales. Estos cambios ayudan a que emerjan nuevos padecimientos, diseminan enfermedades ya existentes a nuevas áreas y aumentan los brotes. En el futuro, enfermedades nuevas podrían traer otras consecuencias imprevistas, como pandemias que impactan ecosistemas enteros.

Vivir en un mundo viral y bacteriano
Los investigadores estiman que todos los virus del mundo, colocados de extremo a extremo, se extenderían a lo largo de 100 millones de años luz. Muchos se originan en animales, que actúan como huéspedes, a veces sin síntomas. Numerosas enfermedades graves han cruzado la barrera de las especies para desencadenar epidemias humanas o pandemias mundiales, incluidas la peste bubónica, la gripe, la malaria, el Ébola, el VIH, la viruela, la tuberculosis, la enfermedad de Lyme, la COVID-19 y muchas más.
“Aproximadamente el 70% de todos los patógenos emergentes y reemergentes son zoonóticos, y no sabemos cuándo surgirá la próxima amenaza, la próxima enfermedad X”, dijo el director general de la Organización Mundial de la Salud (OMS), Tedros Adhanom Ghebreyesus en una reunión sobre la sanidad animal mundial a principios del 2021.
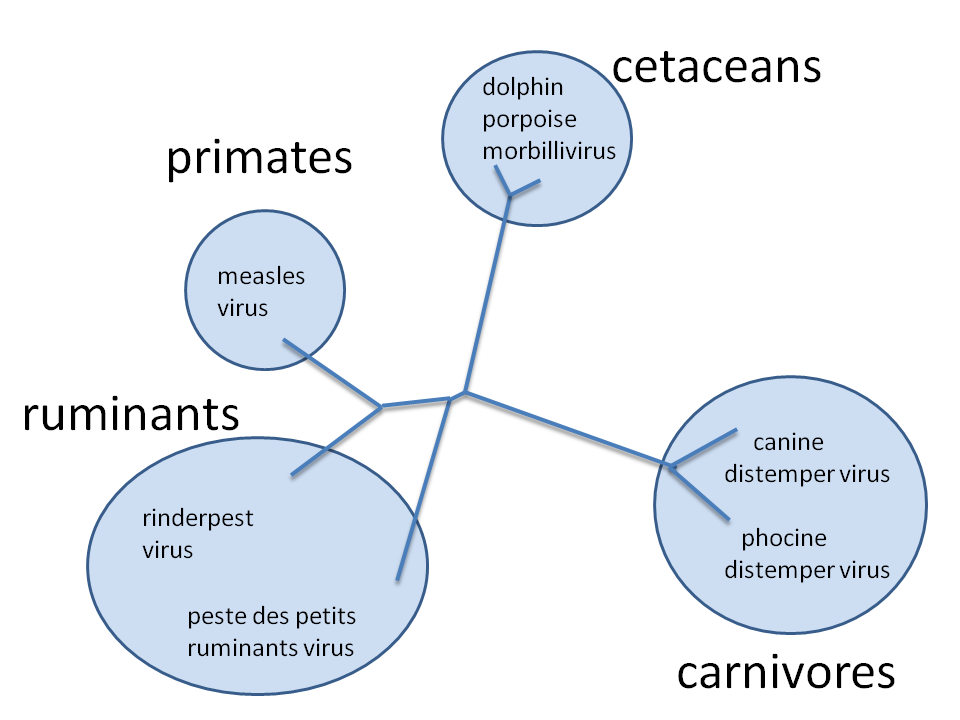
Según el reciente informe “Escapar a la ‘Era de las Pandemias”, se estima que hay 1,7 millones de virus sin descubrir en mamíferos y aves. Todos dependen de huéspedes animales o humanos para reproducirse, propagarse y sobrevivir. La mayoría de las nuevas zoonosis infecciosas han surgido en regiones tropicales, áreas que albergan una rica variedad de especies y los muchos patógenos de los que son huéspedes. China, el sudeste de Asia, India y partes de África son puntos críticos mundiales.
Las enfermedades son parte del mundo natural. Los virus y las bacterias se entrelazan en los ecosistemas en un entorno saludable y diverso, donde los residentes autóctonos han desarrollado defensas que evitan índices devastadores de infección y muerte. Los ecosistemas intactos mantienen el equilibrio: Por ejemplo, la amplia red de vida que prospera en los bosques tropicales normalmente mantiene a los huéspedes de enfermedades, como los roedores, bajo control, dice Rick Ostfeld, ecólogo de enfermedades en el Instituto Cary de Estudios de Ecosistemas en Millbrook, New York.
Ese no es el caso en lugares donde las personas han devastado las poblaciones de animales autóctonos, introducido especies invasoras, troceado o destruido tierras silvestres o instalado animales domésticos en las proximidades de especies salvajes.

El mayor peligro de nuevas pandemias a menudo radica en estos paisajes alterados, dice Chris Walzer, veterinario y director ejecutivo de salud de la Wildlife Conservation Society (WCS) en el Bronx, Nueva York. Cuando los humanos, su ganado y sus perros se instalan en lugares previamente salvajes, esta interconexión antinatural permite a las personas y los animales intercambiar nuevos patógenos infecciosos. Esto crea las condiciones perfectas para que las enfermedades evolucionen y se propaguen a una nueva especie: pueden saltar de los animales a las personas o de las personas a los animales.
Algunos virus, como el de la viruela o del herpes, es raro que se muevan entre especies. Otros virus se adaptan fácilmente y tienen innumerables huéspedes para elegir, dice Billy Karesh, vicepresidente ejecutivo de salud y políticas de EcoHealth Alliance, con sede en Nueva York. La rabia es uno de los virus que mejor se adapta. Se transmite por el mordisco de cualquiera de las 170 especies de mamíferos, incluidos los humanos, y se encuentra en todos los continentes excepto en la Antártida. Sin tratamiento, la inflamación del cerebro resulta invariablemente mortal.
No sabemos la verdadera historia de algunas enfermedades zoonóticas, como el moquillo canino. Los investigadores no están seguros de si los grandes felinos fueron siempre vulnerables. Hubo una breve mención en un artículo en el año 1950 de dos cachorros de león infectados por un cocker spaniel. Entre 1991 y 1992, la enfermedad arrasó en el ahora desaparecido zoológico Wildlife Waystation en California y mató 17 leopardos, tigres y leones y un jaguar. Los biólogos solo se dieron cuenta de la amenaza a la conservación que representa el moquillo canino —y los perros callejeros— cuando un brote en 1994 asoló a los leones del Serengueti (Panthera leo). Alrededor de 1000 leones sucumbieron, una tercera parte de la población en el parque nacional de Tanzania.

El moquillo canino también ha golpeado duramente a otros animales salvajes. El virus ha matado a unas 10 000 focas del Caspio (Phoca caspica); casi exterminó al hurón patinegro (Mustela nigripes) en los Estados Unidos y al lobo etíope (Canis simensis) en África; y ha eliminado manadas enteras de perros salvajes africanos (Lycaon pictus) en peligro crítico de extinción. En 2018, se extendió entre los últimos 600 leones asiáticos (Panthera leo leo). Hoy en día resisten en una franja de bosque en Gujarat, India; una sola epidemia u otro desastre podría acabar con ellos.
El COVID-19 no solo ha golpeado a los humanos; también ha infectado animales. Según los Centros para el Control y la Prevención de Enfermedades de los Estados Unidos, solo en en ese país, visones de criadero, pumas, gorilas, nutrias, leopardos de las nieves y otras especies han sido diagnosticadas con la enfermedad. Este septiembre, los grandes felinos del Zoológico Nacional en Washington D.C. —seis leones africanos, un tigre de Sumatra y dos tigres de Amur— dieron positivo para el virus. Los animales en riesgo ahora están recibiendo una vacuna desarrollada para animales por Zoetis, una empresa mundial de salud animal y aprobada para su uso por el Departamento de Agricultura de los Estados Unidos.

Lee más | Reducción del hielo marino en el Ártico abre nuevas vías a enfermedades en animales
Fomentar una perspectiva de Una Sola Salud
Los veterinarios siempre han sido plenamente conscientes del papel que desempeñan los humanos y los animales en la transmisión de enfermedades entre sí, dice Walzer. Es parte de su educación tradicional: saben que los agricultores pueden contraer enfermedades de los cerdos o las vacas que manejan, dice. También diagnostican regularmente enfermedades que se transmiten entre especies, a veces transmitidas por garrapatas, mosquitos o pulgas. Y, añade, son muy conscientes de que la salud de los animales y las personas está vinculada a la salud del medio ambiente.
Este concepto —conocido indistintamente como Una Sola Salud, salud planetaria o Eco Health— ha adquirido un mayor reconocimiento a lo largo de las dos últimas décadas entre una amplia variedad de expertos, que van desde profesionales médicos y de salud pública hasta economistas que trabajan dentro de los gobiernos, diferentes organizaciones no gubernamentales, la Organización Mundial de la Salud (OMS), las Naciones Unidas y otras organizaciones internacionales.
Sin embargo, los veterinarios y los conservacionistas siguen estando entre los pocos que reconocen claramente una repercusión potencialmente grave de las enfermedades zoonóticas: la extinción. Un brote mortal podría empujar a las especies amenazadas hacia el abismo.
El titi león dorado (Leontopithecus rosalia) en peligro crítico de extinción ofrece un buen ejemplo. En la década de los 80, este primate, endémico del Bosque Atlántico de Brasil, contaba con solo unos pocos cientos en la naturaleza, pero en 2014, los esfuerzos intensivos de conservación restauraron su población a 3700. Luego, en 2018, una epidemia regional de fiebre amarilla en los habitantes de la zona también afectó a los titis y mató a una tercera parte de la población en un solo año.
Entonces, la vacuna humana contra la fiebre amarilla se probó con éxito en titis en cautiverio, lo que ofreció a la especie una nueva esperanza. Los biólogos planean vacunar a 500 de los animales, pero el programa se ha retrasado: los científicos temen infectar a los monos con COVID-19.

África proporciona otro ejemplo de los declives dramáticos que pueden sufrir las especies icónicas debido a las enfermedades, dijo Osofsky. En los años 50, los ganaderos empezaron a cercar enormes áreas para proteger sus rebaños del búfalo salvaje africano, el cual puede albergar la fiebre aftosa, que es altamente contagiosa. Esas cercas bloqueaban antiguas rutas migratorias, lo que impedía el acceso al pastoreo estacional y al agua dulce. Osofsky observó de primera mano lo que él llama “este trágico y costoso conflicto entre el sector del ganado y el sector de la fauna silvestre” cuando desempeñó el cargo de primer veterinario de la fauna silvestre en Botsuana a principios de los años 90. “Cientos de miles, si no millones, de animales salvajes han muerto debido a esas cercas”, dice, incluidos ñus, rinocerontes, cebras y elefantes.
Los mercados de animales salvajes presentan otra importante interconexión de las enfermedades entre humanos y animales, dice Debbie Banks, experta en delitos contra la fauna silvestre de la Agencia de Investigación Ambiental, con sede en Londres. Cada año, millones de animales son extraídos de la naturaleza, legal e ilegalmente, o criados en “granjas de fauna silvestre”. Luego se envían, vivos o en partes, a todo el mundo, dice. Este lucrativo comercio internacional en fauna silvestre está impulsado por la demanda de medicina tradicional china, de carne, pieles, artículos de decoración, joyas y otros productos.
Muchos de estos animales se venden en mercados vivos. Son amontonados unos junto a otros en condiciones insalubres —una cacofonía de animales salvajes entremezclados con cerdos y aves de corral, todos intercambian gérmenes. Estos mercados proporcionan un caldo de cultivo perfecto para que nuevas enfermedades salten especies o para que enfermedades ya existentes se propaguen.

“A los patógenos no les importa si están siendo transportados por un animal que fue comercializado legal o ilegalmente”, apunta Banks.
El comercio legal empequeñece el comercio ilegal, y las condiciones de hacinamiento en las granjas de animales salvajes a escala industrial también representan un riesgo, dice Chris Shepherd, director ejecutivo de Monitor, una organización sin ánimo de lucro que se centra en el comercio de la fauna silvestre. COVID-19 es un ejemplo reciente.
Para principios de enero de 2021, el virus había pasado por al menos 400 granjas de visones a escala industrial en 10 países: los animales habían sido infectados por trabajadores de la granja de pieles. Parece que, en algunos lugares, los visones transmitieron el virus de vuelta a sus cuidadores. A los expertos les preocupa la posibilidad de que se desarrollen nuevas variantes de COVID-19 a medida que la enfermedad salta de un lado para otro entre especies.

Lee más | ¿Un modelo informático para predecir la propagación de enfermedades debido al comercio de mascotas?
Saltar la barrera de las especies: del ganado a la fauna silvestre
Las enfermedades del ganado que infectan a la fauna silvestre son un gran problema de la conservación, dice Karesh, que también es veterinario, algunas desencadenaron mortalidades desastrosas. En 2017, las cabras que compartían tierras de pastoreo con los antílopes saiga de Mongolia (Saiga tatarica mongolica), en peligro crítico de extinción en Mongolia occidental, transmitieron una enfermedad mortal, la peste de los pequeños rumiantes (PPR). El virus devastó la población en solo cuatro meses, de un estimado 25 699 individuos en enero de 2017 a 8806 en mayo.
Al igual que con las pandemias humanas, algunas enfermedades animales se han propagado por los continentes y saltan de la fauna silvestre al ganado y de vuelta a la fauna silvestre. La actual pandemia de peste porcina africana es un ejemplo reciente y sigue siendo una grave preocupación, dice Karesh.
Este virus hemorrágico altamente contagioso e intratable es transportado por facóqueros salvajes (Phacochoerus africanus) y potamóqueros de río (Potamochoerus larvatus) en África; ellos no se ven afectados. Este virus tampoco enferma a las personas, pero para los cerdos de granja es mortal.

En 2007, el virus se trasladó del África subsahariana al país de Georgia y luego a Europa. Ahí, pasó de un lado a otro entre los cerdos de granja y su pariente cercano, el jabalí y mató a los dos. Desde entonces, la peste porcina africana se ha extendido por toda Rusia y alcanzó China en 2018 donde más de 300 millones de cerdos domésticos murieron del virus letal o fueron sacrificados, lo que devastó financieramente a los agricultores y limitó una fuente esencial de proteína.
Ahora se ha infiltrado en el sudeste de Asia, donde pone en peligro a 11 especies de cerdos salvajes sumamente excepcionales. Si el brote continúa propagándose por esa zona, estos cerdos salvajes, con su número limitado y su pequeña gama, podrían ser eliminados con efectos en cascada destructivos para su ecosistema.
Estos cerdos salvajes son los ingenieros de su mundo, labran el suelo, tanto con el fomento como con el control del crecimiento de las plantas y los árboles forestales. Como presas, los cerdos salvajes sustentan a depredadores en peligro crítico de extinción, como los tigres de Sumatra (Panthera tigris sumatrae) y los leopardos de Java (Panthera pardus melas) en Indonesia. Sin cerdos salvajes que comer los grandes felinos entran a las aldeas para ir por el ganado y a menudo acaban muertos, víctimas de una cadena de eventos que empezó con el virus de la peste porcina en África.
Esta es solo una de las muchas, muchas enfermedades zoonóticas que van en ambos sentidos, ya que la fauna silvestre contrae la enfermedad de los animales domésticos y luego lo pasan de vuelta, dice Karesh. Otro ejemplo es la enfermedad de Newcastle, altamente contagiosa, la cual ha sido diagnosticada en más de 240 especies de aves, que van desde pavos y patos silvestres hasta avestruces y aves de corral de granja.
A menudo, también hay daños naturales colaterales en la comunidad que siguen a las muertes causadas por un virus o bacteria. La pérdida de especies clave —dispersores de semillas, depredadores o presas— puede extenderse hacia afuera a través de ecosistemas enteros.

Saltar la barrera de las especies: de los humanos a la fauna silvestre
Alrededor de dos terceras partes de las enfermedades humanas se originan en animales, pero nosotros también los enfermamos. Nuestros parientes más cercanos, los chimpancés, los gorilas y otros primates son especialmente vulnerables: comparten alrededor del 97 % de nuestra composición genética, el resfriado común puede matar a un gorila.
La mayor amenaza a la que se enfrentan los chimpancés en el Parque Nacional Gombe de Tanzania, la tropa que se hizo famosa por la investigadora Jane Goodall, son las enfermedades. En 1966, unos pocos años después de empezar sus estudios, una epidemia de poliomielitis golpeó a los chimpancés de Gombe, más tarde combatieron brotes de gripe y neumonía. Todos resultaron bastante letales, juntos provocaron aproximadamente el 35 % de todas las muertes desde 1960 hasta 2007. Goodall ha dicho que le preocupa la salud de los chimpancés porque a los turistas se les permite acampar en el parque.
Los gorilas de montaña (Gorilla beringei beringei) también están en alto riesgo. Quedan unos 1063 en las montañas africanas de Virunga. Están expuestos regularmente a los guardaparques que los protegen, a los ecoturistas y, ocasionalmente, a los cazadores furtivos. Estos grandes simios han sufrido oleadas de virus respiratorios humanos, a menudo debido a que los turistas se aventuran demasiado cerca, rompen una regla de distanciamiento de 7 metros (23 pies) y pasan sus gérmenes.
Las personas también han propagado la tuberculosis humana al toser o estornudar sobre los orangutanes y otros grandes simios. Los elefantes en cautividad también han contraído la cepa humana y pueden pasárnosla de vuelta; en los elefantes asiáticos, la tuberculosis se instala como una enfermedad crónica y debilitante.

Los mosquitos, garrapatas y pulgas
Los parásitos chupadores de sangre transportan innumerables patógenos que enferman a la fauna silvestre. Los mosquitos portan una gran cantidad de ellos, incluida la fiebre amarilla selvática, que infecta a los monos. En África, de donde es originaria, los simios evolucionaron con la enfermedad, por lo que realmente no se enferman. El virus probablemente emigró a las Américas en barcos de esclavos en la década de 1600; aquí, diezma periódicamente a los monos aulladores marrones (Alouatta guariba clamitans), algunos de los cuales está en peligro de extinción y también amenaza a los titis león dorado.
El área metropolitana de Nueva York se convirtió en la zona cero de otra enfermedad transmitida por mosquitos cuando se registró el primer caso de virus del Nilo Occidental en 1999, una enfermedad identificada en Uganda seis décadas antes. En los años desde su llegada a Nueva York, millones de aves han muerto al migrar el virus por todos los EE. UU., México y el Caribe. Los Centros para el Control y la Prevención de Enfermedades de los Estados Unidos enumeran 412 especies de aves que han dado positivo por el virus del Nilo Occidental. Una vacuna desarrollada para los cóndores de California, en peligro crítico, puede haber salvado a estas raras aves de la extinción.
La misma bacteria que mató a millones de personas durante la “Peste Negra” en la Europa medieval también afecta al reino animal. La peste bubónica, propaganda por las picaduras de pulgas, puede ser mortal para los felinos icónicos, incluidos el león de montaña (Puma concolor), el lince rojo (Lynx rufus) y el lince de Canadá (Lynx canadensis), así como el perro de las praderas y otros animales silvestres.


La estrategia Una Sola Salud es “en nuestro propio interés”
Durante décadas, veterinarios, epidemiólogos, conservacionistas y otros expertos han advertido que perturbar los sistemas naturales planetarios desencadenaría graves impactos perjudiciales para la salud global. Para la fauna silvestre que ya está luchando por sobrevivir en medio de la disminución del hábitat y de las presas, la caza furtiva y el cambio climático, añadir enfermedades a sus riesgos podría inclinar la balanza hacia la extinción.
Hay cada vez un mayor apoyo hacia una estrategia de Una Sola Salud, la cual reconoce que la salud humana, la salud animal y la salud del planeta están inextricablemente vinculadas, que proteger la Tierra es fundamental para la salud de todos.
La actual pandemia ha arrojado una luz brillante sobre el tema y ha atraído la atención del público de una nueva manera, dice Walzer de WCS. “Todo el mundo entiende que hay graves consecuencias y los impactos son altos, así que existe la posibilidad de que ahora haya alguna acción”.
Osofsky está de acuerdo en que la acción rápida es “en nuestro propio interés, lo cual obviamente es siempre un buen motivador para ser mejores administradores de nuestros patios traseros —y el planeta—”.
Referencias:
Gilbert, M., Soutyrina, S. V., Seryodkin, I. V., Sulikhan, N., Uphyrkina, O. V., Goncharuk, M., … Miquelle, D. G. (2015). Canine distemper virus as a threat to wild tigers in Russia and across their range. Integrative Zoology, 10(4), 329-343. doi:10.1111/1749-4877.12137
Quigley, K. S., Evermann, J. F., Leathers, C. W., Armstrong, D. L., Goodrich, J., Duncan, N. M., & Miquelle, D. G. (2010). Morbillivirus infection in a wild Siberian tiger in the Russian Far East. Journal of Wildlife Diseases, 46(4), 1252-1256. doi:10.7589/0090-3558-46.4.1252
Gilbert, M., Sulikhan, N., Uphyrkina, O., Goncharuk, M., Kerley, L., Hernandez Castro, E., … Cleaveland, S. (2020). Distemper, extinction, and vaccination of the Amur tiger. Proceedings of the National Academy of Sciences, 117(50), 31954-31962. doi:10.1073/pnas.2000153117
Myers, S. S., Gaffikin, L., Golden, C. D., Ostfeld, R. S., H. Redford, K., H. Ricketts, T., … Osofsky, S. A. (2013). Human health impacts of ecosystem alteration. Proceedings of the National Academy of Sciences, 110(47), 18753-18760. doi:10.1073/pnas.1218656110
Microbiology by numbers. (2011). Nature Reviews Microbiology, 9(9), 628-628. doi:10.1038/nrmicro2644
Allen, T., Murray, K. A., Zambrana-Torrelio, C., Morse, S. S., Rondinini, C., Di Marco, M., … Daszak, P. (2017). Global hotspots and correlates of emerging zoonotic diseases. Nature Communications, 8(1). doi:10.1038/s41467-017-00923-8
Piat, B. L. (1950). Susceptibility of young lions to dog distemper. Bulletin des Services de l’Élevage et des Industries Animales de A.O.F., 3.
Appel, M. J., Yates, R. A., Foley, G. L., Bernstein, J. J., Santinelli, S., Spelman, L. H., … Summers, B. A. (1994). Canine distemper epizootic in lions, tigers, and leopards in North America. Journal of Veterinary Diagnostic Investigation, 6(3), 277-288. doi:10.1177/104063879400600301
Williams, E. S., Thome, E. T., Appel, M. J., & Belitsky, D. W. (1988). Canine distemper in black-footed ferrets (Mustela nigripes) from Wyoming. Journal of Wildlife Diseases, 24(3), 385-398. doi:10.7589/0090-3558-24.3.385
Goller, K. V., Fyumagwa, R. D., Nikolin, V., East, M. L., Kilewo, M., Speck, S., … Wibbelt, G. (2010). Fatal canine distemper infection in a pack of African wild dogs in the Serengeti ecosystem, Tanzania. Veterinary Microbiology, 146(3-4), 245-252. doi:10.1016/j.vetmic.2010.05.018
Van de Bildt, M. W. (2002). Distemper outbreak and its effect on African wild dog conservation. Emerging Infectious Diseases, 8(2), 212-213. doi:10.3201/eid0802.010314
Seltenrich, N. (2018). Down to Earth: The emerging field of planetary health. Environmental Health Perspectives, 126(7), 072001. doi:10.1289/ehp2374
Dietz, J. M., Hankerson, S. J., Alexandre, B. R., Henry, M. D., Martins, A. F., Ferraz, L. P., & Ruiz-Miranda, C. R. (2019). Yellow fever in Brazil threatens successful recovery of endangered golden lion tamarins. Scientific Reports, 9(1). doi:10.1038/s41598-019-49199-6
Mbaiwa, J. E., & Mbaiwa, O. I. (2006). The effects of veterinary fences on wildlife populations in Okavango Delta, Botswana. International Journal of Wilderness, 12(3), 17-41. Retrieved from http://citeseerx.ist.psu.edu/viewdoc/download?doi=10.1.1.630.7044&rep=rep1&type=pdf
Oude Munnink, B. B., Sikkema, R. S., Nieuwenhuijse, D. F., Molenaar, R. J., Munger, E., Molenkamp, R., … Koopmans, M. P. (2021). Transmission of SARS-CoV-2 on mink farms between humans and mink and back to humans. Science, 371(6525), 172-177. doi:10.1126/science.abe5901
Parida, S., Muniraju, M., Mahapatra, M., Muthuchelvan, D., Buczkowski, H., & Banyard, A. C. (2015). Peste des petits ruminants. Veterinary Microbiology, 181(1-2), 90-106. doi:10.1016/j.vetmic.2015.08.009
Denstedt, E., Porco, A., Hwang, J., Nga, N. T., Ngoc, P. T., Chea, S., … Pruvot, M. (2021). Detection of African swine fever virus in free‐ranging wild boar in Southeast Asia. Transboundary and Emerging Diseases, 68(5), 2669-2675. doi:10.1111/tbed.13964
Luskin, M. S., Meijaard, E., Surya, S., Sheherazade, Walzer, C., & Linkie, M. (2020). African Swine Fever threatens Southeast Asia’s 11 endemic wild pig species. Conservation Letters, 14(3), e12784. doi:10.1111/conl.12784
Ripple, W. J., Estes, J. A., Beschta, R. L., Wilmers, C. C., Ritchie, E. G., Hebblewhite, M., … Wirsing, A. J. (2014). Status and ecological effects of the world’s largest carnivores. Science, 343(6167). doi:10.1126/science.1241484
Patrono, L. V., Samuni, L., Corman, V. M., Nourifar, L., Röthemeier, C., Wittig, R. M., … Leendertz, F. H. (2018). Human coronavirus OC43 outbreak in wild chimpanzees, Côte d’Ivoire, 2016. Emerging Microbes & Infections, 7(1), 1-4. doi:10.1038/s41426-018-0121-2
Williams, J. M., Lonsdorf, E. V., Wilson, M. L., Schumacher‐Stankey, J., Goodall, J., & Pusey, A. E. (2008). Causes of death in the Kasekela chimpanzees of Gombe National Park, Tanzania. American Journal of Primatology, 70(8), 766-777. doi:10.1002/ajp.20573
Mazet, J. A., Genovese, B. N., Harris, L. A., Cranfield, M., Noheri, J. B., Kinani, J. F., … Gilardi, K. V. (2020). Human respiratory syncytial virus detected in mountain gorilla respiratory outbreaks. EcoHealth, 17(4), 449-460. doi:10.1007/s10393-020-01506-8
Moreno, E. S., Agostini, I., Holzmann, I., Di Bitetti, M. S., Oklander, L. I., Kowalewski, M. M., … Miller, P. (2015). Yellow fever impact on brown howler monkeys (Alouatta guariba clamitans) in Argentina: A metamodelling approach based on population viability analysis and epidemiological dynamics. Memórias do Instituto Oswaldo Cruz, 110(7), 865-876. doi:10.1590/0074-02760150075
Lanciotti, R. S., Roehrig, J. T., Deubel, V., Smith, J., Parker, M., Steele, K., … Gubler, D. J. (1999). Origin of the West Nile virus responsible for an outbreak of encephalitis in the Northeastern United States. Science, 286(5448), 2333-2337. doi:10.1126/science.286.5448.2333
Komar, N., & Clark, G. G. (2006). West Nile virus activity in Latin America and the Caribbean. Revista Panamericana de Salud Pública, 19(2), 112-117. doi:10.1590/s1020-49892006000200006
Chang, G. J., Davis, B. S., Stringfield, C., & Lutz, C. (2007). Prospective immunization of the endangered California condors (Gymnogyps californianus) protects this species from lethal West Nile virus infection. Vaccine, 25(12), 2325-2330. doi:10.1016/j.vaccine.2006.11.056
* Imagen principal: Una tigresa de Amur (Panthera tigris altaica) con un cachorro en el zoológico de Búfalo, Nueva York. Imagen de Dave Pape vía Wikimedia Commons (Dominio público).
Artículo original: https://news.mongabay.com/2021/10/in-harms-way-our-actions-put-people-and-wildlife-at-risk-of-disease/
———
Videos | “Aquí va en aumento la deforestación. Si esto sigue así, la mariposa monarca ya no va a llegar”
Si quieres conocer más sobre la situación ambiental en Latinoamérica, puedes revisar nuestra colección de artículos.

Facebook | El problema sigue creciendo: hipopótamos a la venta en Colombia
Si quieres estar al tanto de las mejores historias de Mongabay Latam, puedes suscribirte al boletín aquí o seguirnos en Facebook, Twitter, Instagram y YouTube.
